Udar mózgu jest jedną z najczęstszych i najpoważniejszych przyczyn niepełnosprawności oraz zgonów na świecie. Wymaga natychmiastowej interwencji medycznej, a także kompleksowej opieki pielęgniarskiej na każdym etapie leczenia. W niniejszym wpisie omówimy aspekty opieki pielęgniarskiej nad pacjentem po udarze mózgu.
Spis treści
Definicja udaru mózgu wg American Heart Association/American Stroke Association
Epidemiologia udaru mózgu na świecie
Skale kliniczne do oceny udaru mózgu (GCS, NIHSS, ASPECTS)
Problemy pielęgnacyjne pacjentów po udarze mózgu
Edukacja zdrowotna pacjenta po udarze mózgu
Opieka pielęgniarska nad pacjentem po udarze mózgu
Przykładowy proces pielęgnowania pacjenta po udarze mózgu
Krótka historia udaru mózgu
Pierwsze wzmianki na temat udaru mózgu pojawiły się w literaturze już w 1599 roku. Wówczas określenie to odnosiło się do nagłego wystąpienia objawów, które porównywano do „uderzenia ręki Boga”. Lekarze posługiwali się określeniem „apopleksja”, znanym już od czasów Hipokratesa i przez wiele stuleci stosowanym w diagnostyce tego schorzenia. Termin apopleksja określał stan nagłej utraty świadomości przy zachowanym tętnie i oddechu.
Hipokrates odwołując się do teorii humoralnej (istnienie czterech cieczy (krew, żółta oraz czarna żółć i śluz)), wiązał objawy z zaburzeniem przepływu sił witalnych zawartych we krwi do mózgu.
| „Nie da się wyleczyć silnego ataku apopleksji, a wyleczyć łagodny jest trudno” – Hipokrates |
Postęp nastąpił w XVII wieku dzięki Johanowi Jakobowi Wepferowi, który jako pierwszy powiązał apopleksję z krwotokiem mózgowym, publikując wyniki czterech sekcji w dziele Historiae apoplecticorum (1658).
W kolejnych latach liczba sekcji rosła, a Theophile Bonet w Sepulchretum sive Anatomia Practica (1679) wykazał, że przyczyną udaru mogą być także guz lub ropień mózgu.
Giovanni Morgagni, uznawany za twórcę patologii, w De Sedibus et Causis Morborum Per Anatomen Indagatis (1761) wyróżnił dwie główne postaci apopleksji: „krwistą”, odpowiadającą krwotokowi śródczaszkowemu, oraz „surowiczą”, którą wiązał z nadmiarem płynu mózgowo-rdzeniowego.
Udar mózgu zaczęto postrzegać jako chorobę głównie naczyniową, a stanowisko to wzmocniły odkrycia Johna Abercrombiego i Rudolfa Virchowa. Pierwszy z nich dostrzegł znaczenie okluzji tętnic a drugi przeklasyfikował przyczyny udaru mózgu na krwotoczną i niedokrwienną [1-6].
| Triada Vichrowa – nadmierna krzepliwość krwi, zaburzenia przepływu krwi, uszkodzenie ściany naczynia krwionośnego. |
Definicja udaru mózgu wg WHO
W 1970 r. Światowa Organizacja Zdrowia zdefiniowała udar jako [7]:
| „Szybko rozwijające się objawy kliniczne ogniskowego (lub globalnego) zaburzenia funkcji mózgu, trwające dłużej niż 24 godziny lub prowadzące do śmierci, bez widocznej przyczyny innej niż naczyniowa.” |
Definicja udaru mózgu wg American Heart Association/American Stroke Association
AHA/ASA usunęła czas jako czynnik definiujący i w 2009 r. zatwierdziła obecną definicję przejściowego ataku niedokrwiennego. Brzmi ona: „przejściowy epizod dysfunkcji neurologicznej spowodowany ogniskowym niedokrwieniem mózgu, rdzenia kręgowego lub siatkówki, bez ostrego zawału”.
Przejściowe udary niedokrwienne (TIA) są zazwyczaj określane jako mini udary, których objawy są tymczasowe (tj. trwają od kilku minut do kilku godzin, ale krócej niż 24 godziny) [8].
W 2013 r. AHA/ASA zaktualizowało definicję udaru, która brzmi następująco [9]:
| „Udar mózgu charakteryzuje się deficytem neurologicznym spowodowanym ostrym ogniskowym uszkodzeniem ośrodkowego układu nerwowego (OUN) przez przyczynę naczyniową, w tym zawał mózgu, krwotok śródmózgowy (ICH) i krwotok podpajęczynówkowy (SAH). Jest on główną przyczyną niepełnosprawności i zgonów na całym świecie.” |
Klasyfikacja udaru mózgu
👉 Ze względu na patomechanizm
Ze względu na patomechanizm, można wyróżnić następujące rodzaje udaru mózgu:
1) niedokrwienny – spowodowany skrzepliną w naczyniu krwionośnym (80-85%)
2) krwotoczny, w tym:
– krwotok podpajęczynówkowy (SAH) jest wynikiem krwotoku z naczynia krwionośnego mózgu, tętniaka lub malformacji naczyniowej do przestrzeni podpajęczynówkowej. U pacjentów zazwyczaj występuje nagły początek, silny bólu głowy i wymioty, którym towarzyszą nieogniskowe objawy neurologiczne, takie jak utrata przytomności i sztywność karku. Stanowi około 5% wszystkich udarów.
– krwotok śródmózgowy (ICH) – szybko rozwijające się objawy kliniczne dysfunkcji neurologicznej spowodowane ogniskowym nagromadzeniem krwi w miąższu mózgu lub układzie komorowym, która nie jest spowodowana urazem. ICH stanowi około 10% wszystkich udarów [8].
– inny (5%).
👉 TOAST
Na potrzeby badania Trial of Org 10172 in Acute Stroke Treatment (TOAST) opracowano system klasyfikacji podtypów udaru niedokrwiennego, oparty przede wszystkim na etiologii i mechanizmie niedrożności naczynia.
Podział ten ma istotne znaczenie kliniczne, gdyż wpływa zarówno na dobór strategii leczenia, jak i profilaktyki wtórnej [9].
1. Large-vessel atherothrombosis – w przebiegu chorób dużego naczynia
2. Cardioembolism – udar sercowo-zatorowy
3. Small-vessel disease – w przebiegu chorób małych naczyń
4. Other determined causes – udar o innej etiologii
5. Undetermined causes – udar o nieznanej etiologii
👉 OCSP (Oxfordshire Community Stroke Project)
Klasyfikacja Oxfordshire lub Bamforda opiera się na wynikach badań klinicznych i dzieli udar mózgu ze względu na zajęty obszar, w tym:
– TACI – zawał w całym przednim kręgu unaczynienia (total anterior circulation infarct),
– PACI – zawał w części przedniego kręgu unaczynienia (partial anterior circulation infarct,),
– LACI – zawał lakunarny (lacunar infarction),
– POCI – zawał w tylnym kręgu unaczynienia (posterior circulation infarct) [10].
Przemijający atak niedokrwienny (ang. Transient Ischaemic Attack – TIA) to „udar ostrzegawczy”. Zazwyczaj trwa kilka minut, ale może trwać do 24 godzin. Zwykle pojawia się na kilka godzin lub kilka dni przed udarem i ma podobne objawy.
Epidemiologia udaru mózgu na świecie
Wg danych Global Burden of Disease (GBD) z 2021 roku, udar mózgu pozostaje drugą najczęstszą przyczyną zgonów i trzecią najczęstszą przyczyną niepełnosprawności na świecie.
W 2021 roku udar niedokrwienny mózgu stanowił 65,3%, krwotok śródmózgowy 28,8%, a krwawienie podpajęczynówkowe 5,8% przypadków. Najwyższy odsetek udarów mózgu odnotowano w krajach o wysokich dochodach.
Ponad połowa przypadków udarów wystąpiła u mężczyzn (52,6%), a 47,4% u kobiet.
Badanie wykazało również, że udarom mózgu można w dużym stopniu zapobiegać – 84% przypadków udarów w 2021 roku przypisywało się 23 modyfikowalnym czynnikom ryzyka.
| Dane statystyczne na temat udaru mózgu:
👉 Każdego roku odnotowuje się prawie 12 milionów nowych przypadków udaru. 👉 Co czwarta osoba w populacji globalnej powyżej 25. roku życia dozna udaru mózgu w ciągu swojego życia. 👉 Każdego roku około 15% wszystkich udarów mózgu występuje u osób w wieku 15–49 lat. 👉 Każdego roku około 53% wszystkich udarów mózgu występuje u osób poniżej 70. roku życia. 👉 Co roku około 53% wszystkich udarów mózgu występuje u mężczyzn, a 47% u kobiet. 👉 Na świecie żyje obecnie prawie 94 miliony osób, u których wystąpił udar mózgu. 👉 Ponad 7 milionów ludzi umiera co roku z powodu udaru mózgu [11]. |
Udaru mózgu u Polaków
Zgodnie z danymi przedstawionymi przez NFZ, w 2022 roku w Polsce zanotowano 73,9 tysięcy przypadków udaru niedokrwiennego mózgu. W tym, 89% stanowiły udary pierwszorazowe, a 71,6 tysięcy pacjentów było co najmniej raz hospitalizowanych z powodu udaru niedokrwiennego mózgu.
Ze względu na płeć, 51,4% przypadków udaru dotyczyło mężczyzn, a 44% przypadków dotyczyło populacji powyżej 74 roku życia. Mediana wieku kobiet wynosiła 77 lat a mężczyzn 70 lat.
Najwięcej przypadków odnotowano w województwach śląskim oraz świętokrzyskim, a najmniej w województwach mazowieckim oraz małopolskim [12].
Czynniki ryzyka udaru mózgu
Czynniki ryzyka udaru mózgu można podzielić na modyfikowalne i niemodyfikowalne [10].
| Czynniki | Udar niedokrwienny | Udar krwotoczny |
| Modyfikowalne | – Choroby serca
– Palenie papierosów – Hipercholesterolemia – Hipergomocysteinemia – Cukrzyca – Nadciśnienie tętnicze – Miażdżyca – Otyłość – Niezdrowa dieta – Niska aktywność fizyczna |
– Leczenie przeciwzakrzepowe
– Nadciśnienie tętnicze -Cukrzyca – Nadużywanie alkoholu – Stosowanie narkotyków (szczególnie kokaina i metamfetamina) – Przewlekły stres – Infekcje – Palenie papierosów
|
| Niemodyfikowalne | – Wiek
– Płeć – Rasa/pochodzenie etniczne – Czynniki dziedziczne/rodzinne – Lokalizacja geograficzna |
– Wiek
– Amyloidowa angiopatia – Anomalie naczyń – Rasa/pochodzenie etniczne |
Objawy udaru mózgu
Objawy udaru mózgu różnią się w zależności od zajętego obszaru mózgu (np. krążenie przednie vs krążenie tylne) oraz rodzaju udaru. Objawy podobne w przypadku udaru niedokrwiennego i krwotocznego obejmują:
💊drętwienie lub osłabienie kończyny – udar może spowodować nagłe osłabienie lub drętwienie ręki, często obejmujące tylko jedną stronę ciała. Osoba często ma trudności z uniesieniem jednej ręki lub ręka może mimowolnie opadać.
💊opadanie kącików ust – jednym z charakterystycznych objawów udaru jest osłabienie mięśni twarzy. Zazwyczaj dotyczy to tylko jednej strony twarzy, która może zacząć opadać lub być odrętwiała. Prosty test polega na poproszeniu osoby o uśmiech.
💊 zaburzenia mowy – trudności z mówieniem lub niewyraźna mowa to kolejny wczesny objaw udaru. Osoba może mieć trudności z tworzeniem spójnych zdań, a jej mowa może brzmieć niewyraźnie lub bełkotliwie. Pomocne może być poproszenie o powtórzenie prostego wyrażenia.
💊 nagłe drętwienie lub osłabienie – oprócz twarzy i ramion, drętwienie lub osłabienie może również wystąpić w kończynach dolnych, często obejmując tylko jedną stronę ciała. Osoba może mieć trudności z chodzeniem lub staniem bez utraty równowagi.
💊 dezorientacja i trudności w rozumieniu mowy – u niektórych osób może wystąpić nagła dezorientacja, utrudniająca przetwarzanie informacji lub odpowiadanie na proste pytania. Osoby dotknięte udarem mogą mieć trudności ze zrozumieniem wypowiadanych słów lub instrukcji, nawet jeśli ich słuch pozostaje nienaruszony.
💊 zaburzenia widzenia – udar może wpłynąć na widzenie w jednym lub obu oczach, prowadząc do niewyraźnego lub podwójnego widzenia, a nawet nagłej utraty wzroku w jednym oku. Zaburzenia widzenia często występują wraz z innymi objawami udaru.
💊 zawroty głowy i utrata równowagi – udar może powodować nagłe zawroty głowy, utrudniając osobie dotkniętej udarem utrzymanie równowagi lub powodować zaburzenia koordynacji. Może objawiać się niestabilnym chodzeniem, a nawet upadkami.
💊 silny ból głowy – nagły, silny ból głowy – często określany jako „największy ból głowy w życiu” – jest częstym objawem udaru krwotocznego. Ciśnienie krwi może powodować silny ból, któremu często towarzyszą nudności lub wymioty. W przeciwieństwie do typowego bólu głowy, ból ten pojawia się nagle i bez wyraźnej przyczyny, sygnalizując pilną potrzebę pomocy medycznej [13].
Objawy, które mogą być charakterystyczne dla udaru krwotocznego, obejmują:
💊 napad padaczkowy,
💊 ból lub sztywność karku,
💊 problemy z przełykaniem lub nieprawidłowy smak w ustach,
💊 zwiększoną wrażliwość na światło,
💊 nieregularne bicie serca lub oddychanie.
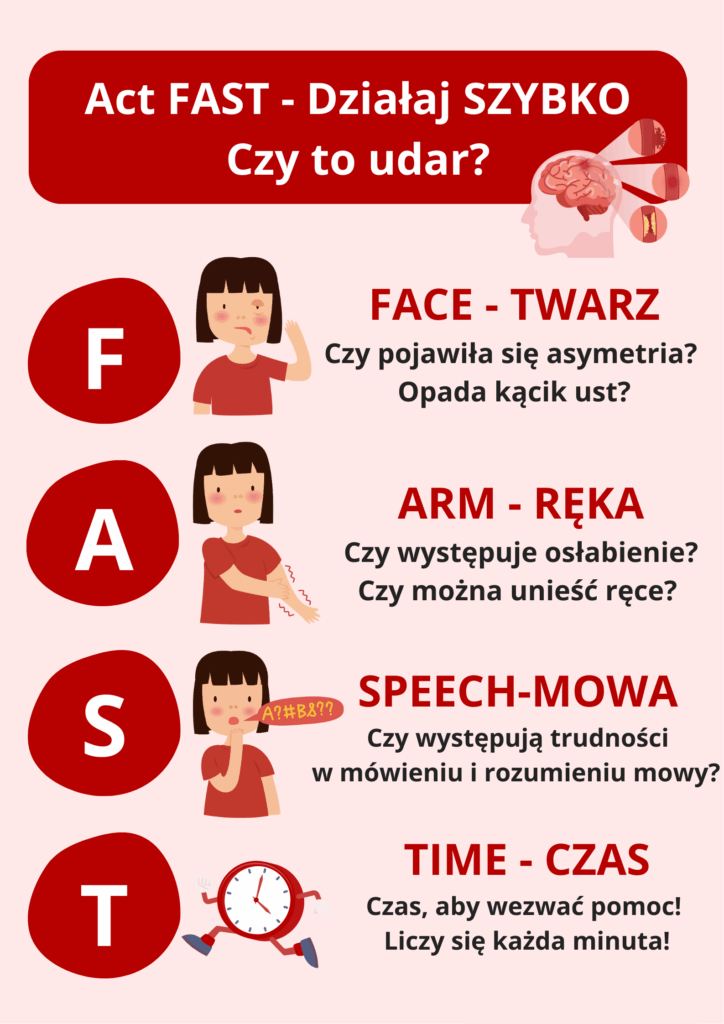
Test FAST – udar mózgu
W lutym 2009 roku rozpoczęto kampanię „Act FAST„, czyli „Działaj szybko”, aby podnieść świadomość na temat objawów udaru i zachęcić ludzi do natychmiastowego kontaktu alarmowego.
Dzięki szybkiej reakcji, osoby z udarem mogą rozpocząć leczenie w ciągu 4,5 godziny od wystąpienia objawów, co zwiększa prawdopodobieństwo trombolizy. FAST pomaga zidentyfikować kluczowe objawy udaru [10].
Prowadzono również badania nad skutecznością rozszerzonej wersji skali – BE FAST, gdzie dodano akronim B – równowaga (balance) oraz E – wzrok (eyesight). Stwierdzono wyższą skuteczność skali FAST [14].
Skala Rosiera
Skala Rosiera to narzędzie kliniczne stosowane do szybkiego rozpoznania udaru mózgu w warunkach ostrych, np. na SOR. Służy do wczesnej selekcji pacjentów [15].
| Objawy | Punkty |
| Utrata przytomności lub omdlenie | -1 |
| Drgawki | -1 |
| Nowy, nagły początek: | |
| Asymetryczne osłabienie mięśni twarzy | +1 |
| Asymetryczne osłabienie kończyny górnej | +1 |
| Asymetryczne osłabienie kończyny dolnej | +1 |
| Zaburzenia mowy | +1 |
| Niedowidzenie / ubytek pola widzenia | +1 |
Czas to mózg
W ludzkim mózgu znajduje się około 130 miliardów neuronów. Jednakże, w każdej minucie, w której pacjent z udarem niedokrwiennym nie otrzymuje leczenia, dochodzi do destrukcji 1,9 miliona neuronów, 14 miliardów synaps i 12 km mielinowych włókien nerwowych.
W przypadku udaru, mózg jest pozbawiony tlenu i liczy się każda minuta. Udar mózgu to stan wymagające natychmiastowego leczenia.
Szybkie leczenie trombolityczne – w ciągu 4,5 godziny, może znacząco poprawić wyniki kliniczne u pacjentów z ostrym udarem niedokrwiennym mózgu, redukując ryzyko nasilenia deficytów neurologicznych [16].
Skale kliniczne do oceny udaru mózgu
GCS
Skala Glasgow Coma Scale (GCS) jest podstawowym narzędziem do oceny neurologicznej pacjentów z ostrym uszkodzeniem mózgu i zaburzeniami świadomości. Skala ocenia reakcje wzrokowe, werbalne i ruchowe [17].
| Reakcja | Stopień zaburzenia | Punkty |
| Otwieranie oczu | spontanicznie | 4 |
| w odpowiedzi na dźwięk | 3 | |
| w odpowiedzi na ból | 2 | |
| brak reakcji | 1 | |
| Odpowiedź słowna | pacjent zorientowany odpowiada poprawnie | 5 |
| odpowiadanie, ale pacjent jest zdezorientowany | 4 | |
| niepoprawne słowa | 3 | |
| niezrozumiałe dźwięki | 2 | |
| brak reakcji | 1 | |
| Odpowiedź ruchowa | wykonuje polecenia | 6 |
| właściwe umiejscowienie bólu | 5 | |
| wycofanie w odpowiedzi na ból | 4 | |
| nieprawidłowa reakcja zgięciowa na ból | 3 | |
| zwiększona reakcja wyprostna na ból | 2 | |
| brak reakcji | 1 |
NIHSS
Skala NIHSS jest używana na całym świecie. Najczęściej stosuje się ją w przypadku ostrego udaru niedokrwiennego mózgu, ale jest również wykorzystywana do oceny pacjentów po udarze krwotocznym lub z podejrzeniem przemijającego ataku niedokrwiennego mózgu.
Skala służy do oceny stanu pacjenta w ostrej fazie leczenia, oceny skuteczności leczenia i przewidywania wyników leczenia [18].
| Przytomność | 0 – przytomny
1 – podsypiający, wybudza się podczas bodźców 2 – nieprzytomny, wymaga wielokrotnej stymulacji 3 – brak odruchów i reakcji na bodźce |
| Pytanie o wiek i miesiąc | 0 – obie odpowiedzi prawidłowe
1 – jedna odpowiedź jest prawidłowa 2 – obie odpowiedzi są nieprawidłowe |
| Wykonywanie poleceń | 0 – oba polecenia wykonane prawidłowo
1 – jedno polecenie wykonane prawidłowo 2 – żadne polecenie nie jest wykonane prawidłowo |
| Ruchomość gałek ocznych | 0 – prawidłowa
1 – częściowe porażenie 2 – całkowite porażenie |
| Pole widzenia | 0 – bez zaburzeń
1 – częściowe niedowidzenie połowicze 2 – całkowite niedowidzenie połowicze 3 – obustronne niedowidzenie połowicze |
| Porażenie nerwu twarzowego | 0 – prawidłowe ruchy
1 – niewielki niedowład 2 – częściowe porażenie 3 – całkowite porażenie |
| Siła mięśni kończyn górnych | 0- nie opada
1 – opada, chory utrzymuje kończynę pod kątem 45 lub 90° >10 s 2- częściowy ruch 3- brak ruchu, kończyna opada 4 – brak ruchu 5 – amputacja |
| Siła mięśni kończyn górnych | 0- pacjent utrzymuje kończynę pod kątem 30° przez 5 seskund
1- opada powoli 2- opada szybko (zachowany opór) 3- opada natychmiast, 4 – brak ruchu 5 – amputacja lub blok w stawi |
| Ataksja kończyn | 0 – brak
1-w jednej kończynie 2-w obu kończynach 3-amputacja |
| Czucie | 0-obecne
1-częściowa utrata czucia 2-całkowita utrata czucia |
| Mowa | 0-brak afazji
1-afazja łagodna do umiarkowanej 2-afazja dużego stopnia 3-afazja całkowita |
| Dyzartia | 0-brak
1-łagodna do umiarkowanej 2-ciężka 3-chory zaintubowany |
| Reakcja na bodźce | 0-prawidłowa
1-brak reakcji na jeden z bodźców (czucie, słuch, wzrok) 2- brak rozróżnienia więcej niż jednego bodźca |
ASPECTS
W praktyce klinicznej wykorzystuje się często skalę ASPECTS w kierunku różnicowania udaru niedokrwiennego mózgu. Jej celem jest identyfikacja chorych z największym potencjałem osiągnięcia korzyści terapeutycznych w okresie trzech miesięcy po otrzymaniu dożylnego leczenia trombolitycznego oraz oszacowania ryzyka zdarzeń niepożądanych. Pozwala ona oszacować między innymi ryzyko wystąpienia krwawienia wewnątrzczaszkowego po terapii trombolitycznej. Skala obejmuje zakres punktowy 0-10:
– 0-4 – udar duży,
– 5-7 – udar umiarkowany,
– 8-10 udar mały [19].
Problemy pielęgnacyjne pacjentów po udarze mózgu
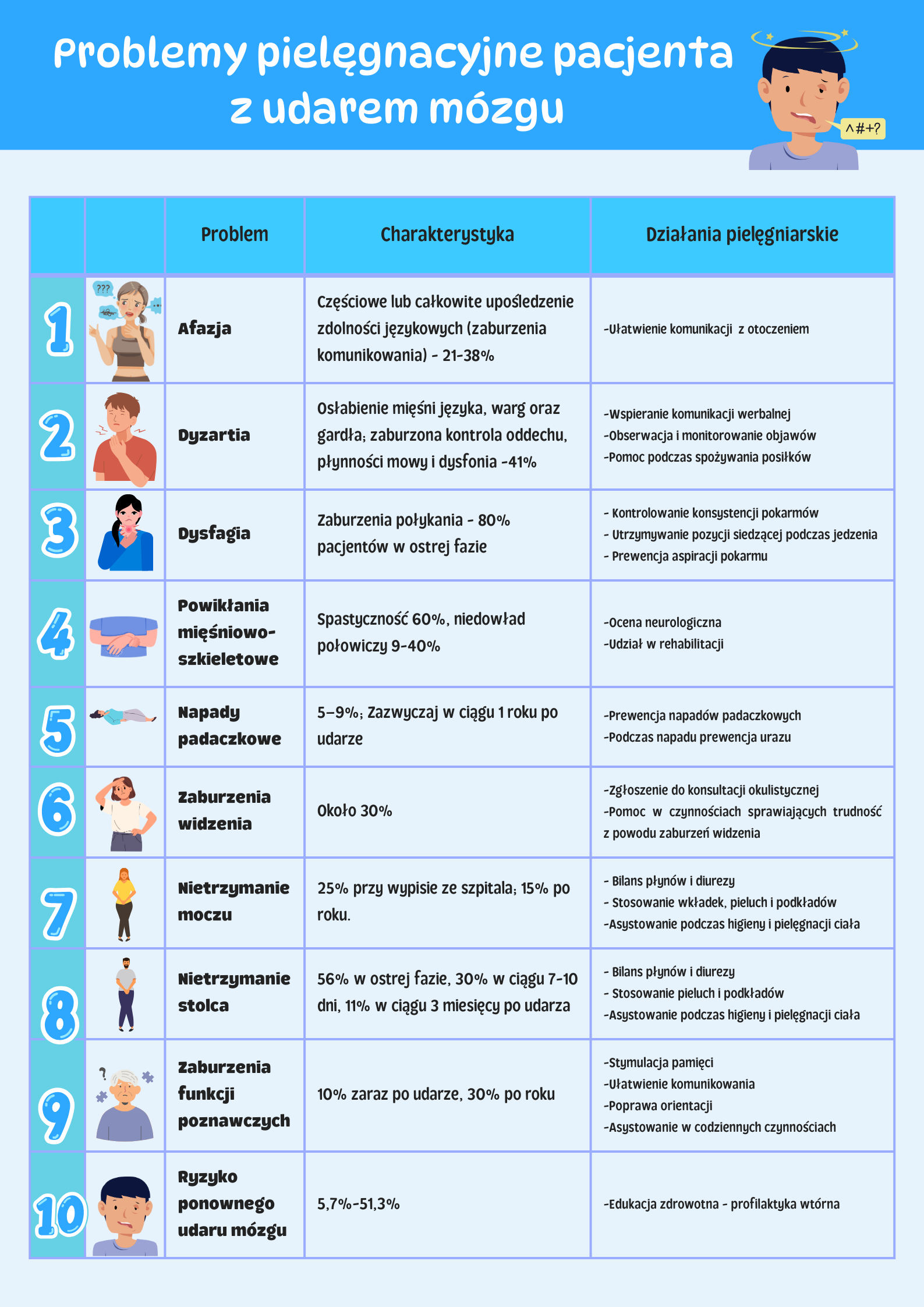
Udar mózgu stanowi jedną z głównych przyczyn niepełnosprawności wśród dorosłych, prowadząc do licznych zaburzeń funkcji organizmu. Pacjenci po przebytym udarze wymagają kompleksowej opieki pielęgniarskiej, ukierunkowanej na rozwiązywanie problemów zdrowotnych i poprawę jakości życia. Zerknij na poniższy przegląd potencjalnych problemów pielęgnacyjnych u pacjentów po udarze mózgu.
Afazja
Afazja to częściowe lub całkowite upośledzenie zdolności językowych, które występuje w wyniku uszkodzeń różnych obszarów kory mózgowej. Afazja może pojawić się u pacjenta po udarze mózgu. Wyróżnia się kilka rodzajów afazji, w zależności od uszkodzonego obszaru mózgu. Zaburzenie to dzieli się na afazję ruchową oraz czuciową [20].
| Rodzaj | Zaburzenia funkcji językowych | Uszkodzony obszar mózgu |
| Afazja Broca (Broki) | Zaburzenia produkcji mowy
Powtarzanie słów |
Ośrodek Broca
(płat czołowy) |
| Afazja Wernick’ego (Wernickiego) | Zaburzenia rozumienia mowy
Powtarzanie słów |
Ośrodek Wernick’ego
(obszar Brodmana 22, płat skroniowy) |
| Afazja przewodzeniowa | Zaburzenia płynnej mowy spontanicznej | Pęczek łukowaty |
| Afazja całkowita | Ciężkie upośledzenie produkcji i zrozumienia mowy | Ośrodek Broca i Wernickego |
| Afazja nominalna (anomiczna) | Zaburzenia mowy spontanicznej
Trudności z powtarzaniem słów Trudności ze zrozumieniem języka |
Różne części płata ciemieniowego lub płata skroniowego |
| Afazja transkorowa motoryczna (ruchowa) | Brak płynności mowy
Hipofonia Perseweracja Echolalia Trudności z powtarzaniem słów |
Przednia górna część płata czołowego dominującej półkuli mózgu |
| Afazja transkorowa sensoryczna (czuciowa) | Trudności ze znajdowaniem słów
Trudności ze zrozumieniem mowy |
Dolny lewy płat skroniowy |
| Afazja transkorowa mieszana | Trudności ze znajdowaniem słów
Trudności ze zrozumieniem mowy Brak płynności mowy Aleksja Agrafia |
Tylny obszar ośrodka Wernickego (płata skroniowego lub pogranicza płata ciemieniowego) |
Dyzartia
Dyzartria jest częstym objawem występującym na skutek udaru i stanowi przyczynę upośledzenia czynnościowego u pacjentów. Diagnozuje się ją u około 41% osób po udarze. Jest to neuromotoryczne zaburzenie mowy wynikające z uszkodzenia śródczaszkowych struktur nerwowych. Można podzielić ją na następujące rodzaje:
– wiotka – osłabienie mięśni np. języka, ust, żuchwy, policzków,
– spastyczna – hipertonia, trudności z mówieniem, spowolniona mowa, rozciąganie słów,
– ataktyczna – trudności z koordynacją, niezborność ruchowa,
– hipokinetyczna – sztywność mięśni aparatu mowy, monotonna, niewyraźna i spowolniona mowa, trudności z rozumieniem mowy,
– hiperkinetyczna – mimowolne ruchy,
– jednostronna górnego neuronu ruchowego,
– mieszana – porażenie opuszkowe, porażenie rzekomoopuszkowe, stwardnienie zanikowe boczne, zaburzenia móżdżkowe, parkinsonizm, dystonia, pląsawica.
Dyzartria charakteryzuje się osłabieniem mięśni języka, warg oraz gardła, a także zaburzoną kontrolą oddechu, płynności mowy i dysfonią [21].
Dysfagia
Dysfagia ustno-gardłowa dotyczy 80% pacjentów w ostrej fazie udaru mózgu. Jest to negatywny czynnik prognostyczny poprawy stanu neurologicznego pacjenta. Na skutek zaburzeń połykania, u pacjenta może dojść do niedożywienia, odwodnienia, zachłystowego zapalenia płuc, obniżenia jakości życia, a nawet zgonu [22].
Napady padaczkowe
Napady padaczkowe po udarze występują u 5–9% wszystkich osób po udarze. Większość napadów padaczkowych występuje w ciągu pierwszego roku od udaru. Rzadko zdarza się, aby napady wystąpiły po upływie dwóch lat od wystąpienia udaru. Występują one częściej po udarze krwotocznym, udarze z powodu całkowitego zajęcia krążenia przedniego oraz udarze z zajęciem kory mózgowej. Należy je leczyć lekami przeciwdrgawkowymi [23].
Nietrzymanie moczu
Po udarze pacjenci często doświadczają różnego stopnia częstomoczu, parcia naglącego lub nietrzymania moczu z powodu pęcherza neurogennego, co prowadzi do niepełnego opróżniania pęcherza. Dokładny mechanizm nietrzymania moczu po udarze jest niejasny.
Około 25% pacjentów po udarze dotyka nietrzymanie moczu przy wypisie ze szpitala, a 15% pacjentów zmaga się z tym problemem po roku. Nietrzymanie moczu po 30 dniach od udaru wiąże się z prawie czterokrotnie większą śmiertelnością w ciągu roku.
Postępowanie terapeutyczne obejmuje wykluczenie czynników zaostrzających/wyzwalających, w szczególności infekcji dróg moczowych. Leki antycholinergiczne mogą być stosowane w celu zmniejszenia parcia naglącego i częstomoczu. Inną metodą terapeutyczną jest zastosowanie cewnika lub wkładek/pieluch [23].
Nietrzymanie stolca
Nietrzymanie stolca po udarze jest bardzo częste i występuje u 56% przypadków w ostrej fazie, u 30% osób w ciągu 7-10 dni i u 11% w ciągu trzech miesięcy. Najbardziej narażeni są pacjenci starsi, kobiety i osoby z ciężkim udarem [23].
Zaburzenia funkcji poznawczych
Udar stanowi częstą przyczynę zaburzeń funkcji poznawczych i demencji w późniejszym wieku. Demencja jest drugą najczęstszą formą zaburzeń poznawczych po chorobie Alzheimera. U około 10% pacjentów zaburzenia funkcji poznawczych rozwijają się od razu po udarze, a u około 30% po roku od wystąpienia udaru. Czynniki ryzyka rozwoju demencji obejmują podeszły wiek, przebyty udar, udar lakunarny, cukrzycę i udar lewej półkuli mózgu [23].
Powikłania mięśniowo-szkieletowe
Zaburzenia mięśniowo-szkieletowe po udarze zazwyczaj obejmują jedną połowę ciała i mogą ujawnić się dopiero po kilku tygodniach lub miesiącach.
Objawy związane ze spastycznością występują nawet u 60% pacjentów po udarze. Spastyczność to nadmierna, nieadekwatna i mimowolna aktywność mięśni, prowadząca do sztywności, utraty ruchomości i bólu. W najgorszym przypadku prowadzi do trwałej deformacji zwanej przykurczem.
Ból barku wywołany niedowładem połowiczym występuje u 9%–40% przypadków pacjentów po udarze i zwykle pojawia się 2–3 miesiące po wystąpieniu udaru [23].
U pacjentów może wystąpić również niedowład lub paraliż. Często dotyka kończyny górnej, lecz może dotyczyć również twarzy [24, 25].
Zaburzenia zdrowia psychicznego
Psychospołeczne powikłania udaru mózgu dotykają większości pacjentów, wywierając negatywny wpływ zarówno na pacjenta, jak i na jego najbliższe otoczenie, rodzinę i przyjaciół. Do częstych zaburzeń na tle zdrowia psychicznego u pacjentów po udarze mózgu zaliczają się depresja, niestabilność emocjonalna oraz wahania nastroju [23].
Zaburzenia widzenia
Około 30% pacjentów po udarze cierpi na upośledzenie funkcji wzroku. Najczęstsze jest niedowidzenie połowicze, ale często występują również podwójne widzenie, obniżona ostrość wzroku, opadanie powieki, anizokoria i oczopląs. Mimo iż u części pacjentów możliwe jest częściowe lub całkowite wyleczenie zaburzeń widzenia, u wielu pacjentów dochodzi do trwałej niepełnosprawności w zakresie widzenia [26].
Ryzyko ponownego udaru mózgu
Jednym z poważnych zagrożeń dla pacjentów po przebytym udarze mózgu jest ryzyko ponownego udaru. W literaturze przedmiotu częstość tego zjawiska szacuje się różnie – od 5,7% do nawet 51,3%. Kluczowe znaczenie ma edukacja zdrowotna pacjentów w zakresie profilaktyki wtórnej.
Szczególną rolę odgrywa tu zachęcanie do przestrzegania zaleceń pielęgniarskich i lekarskich, a także podejmowania prozdrowotnych zachowań, takich jak kontrola ciśnienia tętniczego, kontrola chorób współistniejących, właściwa dieta, regularna aktywność fizyczna czy unikanie używek [27].
Leczenie i farmakoterapia
Leczenie zależy od rodzaju udaru, czasu od wystąpienia objawów oraz stanu klinicznego pacjenta. W przypadku udaru niedokrwiennego mózgu stosuje się leczenie trombolityczne lub trombektomię mechaniczną.
Leczenie trombolityczne polega na podaniu leku rozpuszczającego skrzep. Trombektomia mechaniczna to zabieg wewnątrznaczyniowy polegający na mechanicznym usunięciu skrzepliny. Wytyczne dotyczące leczenia ostrego udaru zalecają wdrożenie następujących leków w postepowaniu z pacjentami u których wystąpił udar niedokrwienny mózgu:
– aspiryna (ASA),
– tkankowy aktywator plazminogenu (tpa),
– leki przeciwzakrzepowe, w tym heparyna lub warfaryna,
– leki przeciwnadciśnieniowe,
– środki obniżające stężenie lipidów [28].
W przypadku udaru krwotocznego, leczenie obejmuje obniżenie ciśnienia wewnątrzczaszkowego. W zależności od przyczyny krwawienia, wdraża się leczenie chirurgiczne lub wewnątrznaczyniowe. Dwa główne przyczyny osłabienia naczyń krwionośnych, które zazwyczaj powodują udar krwotoczny to tętniaki i malformacje tętniczo-żylne (AVM). Najczęstszą przyczyną udaru krwotocznego jest niekontrolowane nadciśnienie tętnicze.
Rehabilitacja neurologiczna
Istotną rolę w procesie terapeutycznym odgrywa również rehabilitacja. Przebieg rehabilitacji jest zależny od stopnia niepełnosprawności pacjenta – lekki, umiarkowany, znaczny. Celem rehabilitacji jest pomoc w odzyskaniu jak najwyższego stopnia sprawności fizycznej.
Ocena pacjenta po udarze obejmuje szczegółową analizę stanu neurologicznego, w tym funkcji motorycznych, czuciowych, koordynacji i zdolności poznawczych. Pomaga ona w szybkim zidentyfikowaniu wszelkich deficytów lub upośledzeń wynikających z udaru.
Ponadto, wczesna ocena zdolności mowy i połykania jest kluczowa, gdyż pomaga w identyfikacji wszelkich zaburzeń komunikacji lub dysfagii, wskazując na potrzebę specjalistycznej konsultacji.
Kluczowym okresem po wystąpieniu udaru jest czas rekonwalescencji. Można go podzielić na kilka faz, w tym:
– pierwsze 24 godziny po udarze – faza nadostra,
– pierwsze 7 dni po udarze – faza ostra,
– miesiące po udarze – wczesna faza podostra,
– 4–6 miesięcy po udarze – późna faza podostra,
– od 6 miesiąca po udarze – faza przewlekła [29].
Można wyróżnić rehabilitację wczesną – przyłóżkową oraz rehabilitację późną, która dotyczy pacjentów po zakończeniu okresu hospitalizacji oraz stanów przewlekłych.
Rehabilitacja obejmuje:
– uruchomienie pacjenta,
– pionizację,
– profilaktykę przeciwodleżynową,
– prewencję przeciwobrzękową,
– profilaktykę przeciwprzykurczową,
– adaptację do wysiłku fizycznego,
– edukację chorego i rodziny [30, 31].
Edukacja zdrowotna pacjenta po udarze mózgu
Pacjenci po udarze wymagają wsparcia i wskazówek dotyczących poprawy zachowań związanych z samoopieką, aby mogli skuteczniej radzić sobie ze swoim stanem zdrowia oraz zmniejszać ryzyko wystąpienia kolejnego udaru mózgu.
Edukacja zdrowotna prowadzona przez pielęgniarki ma na celu rozwój umiejętności pacjenta oraz wsparcie w planowaniu i wdrażaniu samodzielnej opieki po zakończeniu hospitalizacji. Dotyczy to zarówno chorego, jak i jego rodziny.
Szczególny nacisk należy położyć na edukację w zakresie samoopieki i samopielęgnacji, w tym działania w zakresie profilaktyki wtórnej. Ponowny udar często wiąże się z poważniejszym uszkodzeniem mózgu, co może prowadzić do licznych powikłań i pogorszenia rokowania.
Aby ograniczyć ryzyko nawrotu choroby, konieczne jest monitorowanie oraz redukcja lub eliminacja czynników ryzyka, takich jak nadciśnienie tętnicze, hipercholesterolemia, cukrzyca, otyłość, brak aktywności fizycznej czy przewlekły stres [32].
Opieka pielęgniarska nad pacjentem po udarze mózgu

Na początku warto określić model opieki pielęgniarskiej. Następnie należy ustalić czy wykorzystać IV-etapowy czy V-etapowy model pielęgnowania. Dowiedz się więcej na temat procesu pielęgnowania i diagnoz pielęgniarskich. Podczas tworzenia diagnoz warto oprzeć się o klasyfikację NANDA-I oraz ICNP.
🧬 Przykład:
Diagnoza pielęgniarska aktualna wg PES (problem – etiologia – symptom).

|
Diagnoza pielęgniarska Zaburzenia komunikacji werbalnej (P) związane z uszkodzeniem neurologicznym wpływającym na ośrodki mowy (np. obszar Broki lub Wernickiego) (E) dyzartrią (E) deficytami poznawczymi wpływającymi na przetwarzanie języka i znajdowanie odpowiednich słów (E) objawiające się niezdolnością do tworzenia słów lub zdań (afazja ekspresyjna) (S) niezdolnością do rozumienia języka mówionego lub pisanego (afazja receptywna) (S) niewyraźną lub niezrozumiałą mową (dyzartria) (S) frustracją lub lękiem związanym z trudnościami w komunikacji (S) |
Kolejnym krokiem jest określenie celu działań pielęgniarskich.
🧬Przykład:
|
Cel działań: Poprawa komunikacji werbalnej i rozumienia języka przez pacjenta w okresie hospitalizacji. Umiejętność skutecznego komunikowania podstawowych potrzeby przez pacjenta z użyciem metod werbalnych lub niewerbalnych. Redukcja lub eliminacja frustracji i lęku związanych z trudnościami w komunikacji. |
Następne elementy procesu pielęgnowania obejmują ułożenie planu opieki oraz jego realizację. Spójrz poniżej na przykładowe działania pielęgniarskie związane z zaburzeniami mowy u pacjenta po udarze mózgu.
🧬Przykład:
|
Działania pielęgniarskie: Ułatwienie skutecznej komunikacji – używanie krótkich, jasnych zdań, zapewnienie dodatkowego czasu na odpowiedź, zadawanie jednego pytania na raz, weryfikowanie zrozumienia poprzez powtarzanie lub parafrazowanie, zachęcanie do korzystania z gestów, tablic komunikacyjnych lub urządzeń elektronicznych. Terapia w zakresie mowy – współpraca z logopedą w celu uzyskania indywidualnej terapii, ćwiczenie artykulacji, płynności mówienia i rozumienia języka, zachęcanie do powtarzania powszechnie używanych słów, fraz lub poleceń. Promowanie alternatywnych metod komunikacji – korzystanie z tablic komunikacyjnych i kart obrazkowych w celu zaspokojenia podstawowych potrzeb (np. jedzenia lub bólu), włączanie elektronicznych urządzeń komunikacyjnych lub aplikacji generujących mowę. Wsparcie emocjonalne i strategie radzenia sobie – zapewnianie poczucia pewności i wsparcia emocjonalnego w celu zmniejszenia frustracji i lęku, edukowanie rodziny i opiekunów na temat skutecznych strategii komunikacji. |
Na koniec, należy wskazać wynik podjętych działań pielęgniarskich.
🧬Przykład:
|
Ocena podjętych działań: Pacjent skutecznie komunikował swoje potrzeby w okresie hospitalizacji drogą werbalną i niewerbalną. Pacjent zgłosił obniżenie poczucia frustracji i leku w związku z trudnościami w komunikacji. |
Możesz wykorzystać również formę tabeli (Model IV-etapowy) oraz stworzyć proces z wykorzystaniem kodów ICNP.
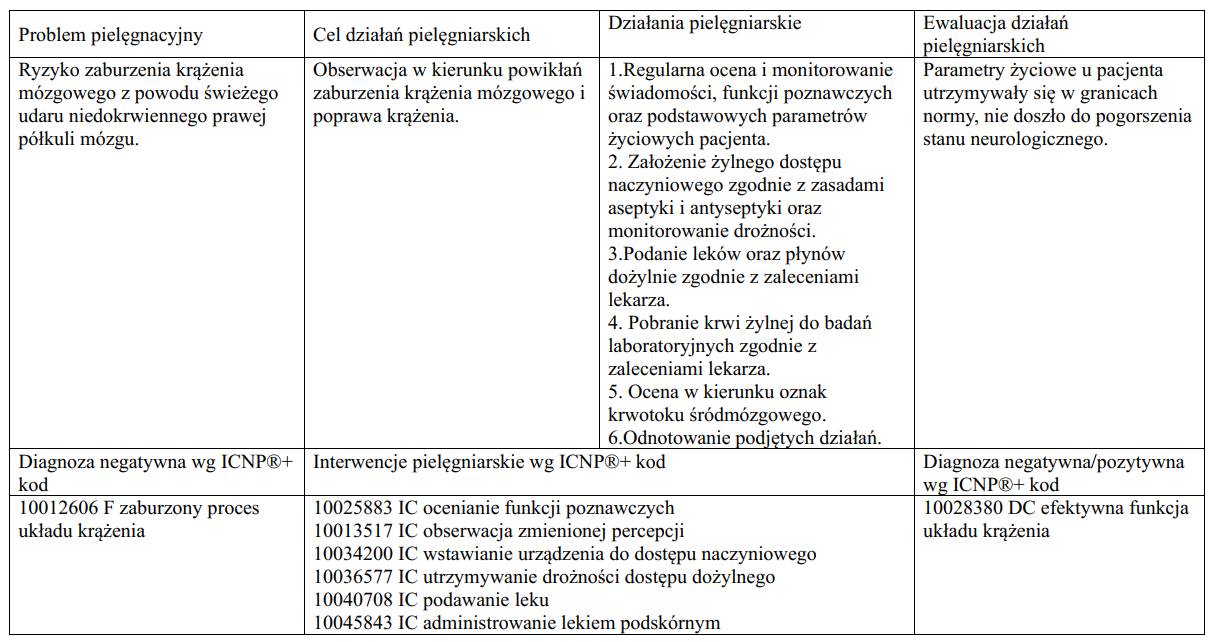
🧬Przykład:
| Problem pielęgnacyjny | Cel działań pielęgniarskich | Działania pielęgniarskie | Ewaluacja działań pielęgniarskich |
| Trudności w komunikacji z otoczeniem spowodowane afazją mieszaną objawiające się trudnością z wypowiadaniem słów. | Zapewnienie metod pozwalających na efektywne komunikowanie z otoczeniem. | 1.Ocena barier komunikacyjnych, zarówno werbalnych, jak i niewerbalnych.
2.Ustalenie z pacjentem sposobów ułatwiających komunikację z otoczeniem, w tym formułowanie krótkich pytań i odpowiedzi, a także wykorzystywanie mimiki i gestykulacji, w celu komunikowania potrzeb i uczuć. 3.Okazanie cierpliwości oraz wsparcia emocjonalnego podczas komunikacji. 4.Odnotowanie podjętych działań. |
Pacjent może skutecznie przekazywać informacje i potrzeby. |
| Diagnoza negatywna wg ICNP®+ kod | Interwencje pielęgniarskie wg ICNP®+ kod | Diagnoza negatywna/pozytywna wg ICNP®+ kod | |
| 10025104 DC zaburzona komunikacja werbalna | 10009683 IC identyfikowanie przeszkody w komunikacji
10030515 IC ocenianie zdolności komunikowania werbalnego 10036169 IC nauczanie o efektywnym komunikowaniu 10038196 IC ułatwianie komunikowania potrzeb 10026616 IC ułatwianie komunikowania uczuć 10027051 IC zapewnienie wsparcia emocjonalnego |
10028230 DC zdolna/y do komunikowania werbalnego
10025025 DC zdolny/a do komunikowania |
|
Zerknij poniżej na kilka przykładowych problemów pielęgnacyjnych i działań pielęgniarskich u pacjenta po udarze mózgu [33,34].
🧬Przykład:
Diagnoza pielęgniarska. Dysfagia wywołana udarem niedokrwiennym mózgu objawiająca się trudnościami w spożywaniu posiłków.
Cel opieki pielęgniarskiej: Zwiększenie komfortu pacjenta podczas spożywania posiłku oraz prewencja aspiracji pokarmu.
Plan opieki pielęgniarskiej:
1. Ocena zdolności pacjenta do spożywania posiłku.
2. Asystowanie pacjentowi podczas spożywania posiłku.
3. Płynoterapia.
4. Edukacja w zakresie spożywania pokarmu.
5. Edukacja w zakresie prawidłowego nawodnienia organizmu.
6. Asystowanie podczas higieny jamy ustnej po posiłku.
7. Udokumentowanie podjętych czynności.
Realizacja planu opieki pielęgniarskiej:
1. Pacjent zgłosił trudności z przełykaniem, co utrudniało mu przyjmowanie posiłków.
2. Asystowano w przyjęciu pozycji siedzącej i spożywaniu posiłków – podawano małe porcje pokarmu, unikano twardych i suchych produktów. Zadbano o konsystencję płynną lub papkowatą posiłków.
3. Wdrożono płynoterapię iv. oraz podawano płyny w niewielkich ilościach.
4. Zalecono spożywanie pokarmu w spokoju oraz powolne i dokładne żucie.
5. Poinformowano o konieczności przyjmowania odpowiedniej ilości płynów, w celu prewencji odwodnienia.
6. Po każdym posiłku asystowano pacjentowi podczas wykonywania higieny jamy ustnej.
7. Udokumentowano podjęte działania w Karcie Obserwacji Pielęgniarskich.
Ocena podjętych działań pielęgniarskich:
Pacjent zwiększył komfort podczas jedzenia, nie doszło do aspiracji pokarmu.
🧬Przykład:
| Problem pielęgnacyjny | Działania pielęgniarskie |
| Niedowład lub paraliż kończyn / osłabienie siły mięśniowej | – Udział w rehabilitacji
– Pomoc w zmianie pozycji ciała – Pomoc w pionizacji oraz przemieszczaniu się – Stosowanie sprzętu wspomagającego |
| Ryzyko zaburzeń układu krążenia | – Monitorowanie podstawowych parametrów życiowych
– Ocena neurologiczna pacjenta – Podawanie leków zgodnie z zaleceniami lekarza |
| Zaburzenia mowy i komunikacji | – Stosowanie prostego języka, krótkich zdań
– Zachęcanie do mówienia i gestykulacji – Współpraca z logopedą |
| Trudności w połykaniu (dysfagia) | – Kontrolowanie konsystencji pokarmów
– Utrzymywanie pozycji siedzącej podczas jedzenia – Prewencja aspiracji pokarmu |
| Problemy z równowagą i koordynacją | – Pomoc przy pionizacji i poruszaniu się
– Zapewnienie bezpiecznego środowiska (np. poręcze, chodzik) |
| Ryzyko powikłań zakrzepowo-zatorowych | – Mobilizacja pacjenta
– Stosowanie pończoch uciskowych – Monitorowanie obrzęków i bólu kończyn – Udział w farmakoterapii |
| Zmiany emocjonalne i psychiczne | – Aktywne słuchanie
– Wsparcie emocjonalne – Przekazanie informacji o możliwości udziału w terapii grupowej – Obserwacja objawów depresji lub lęku – Okazywanie wsparcie emocjonalnego |
| Nietrzymanie moczu lub stolca | – Bilans płynów i diurezy
– Stosowanie wkładek, pieluch i podkładów – Asystowanie podczas higieny i pielęgnacji ciała |
| Dolegliwości bólowe głowy | – Ocena nasilenia dolegliwości bólowych
– Podanie środków przeciwbólowych zgodnie z zaleceniami lekarza – Regularna ocena nasilenia dolegliwości, skutków ubocznych i samopoczucia pacjenta |
| Ryzyko ponownego udaru / Deficyt wiedzy na temat profilaktyki | – Ocena poziomu wiedzy
– Edukacja zdrowotna pacjenta i rodziny w zakresie profilaktyki wtórnej udaru |
| Ograniczona zdolność do samoopieki | – Ocena zdolności do samoopieki i samopielęgnacji np., skala Becka, ADL
– Asystowanie w czynnościach higienicznych, pielęgnacyjnych, poruszaniu i spożywaniu posiłków |
Zerknij na bardziej rozbudowany przykładowy opis przypadku i proces pielęgnowania pacjenta po udarze niedokrwiennym mózgu.
Przykładowy proces pielęgnowania pacjenta po udarze mózgu
Jeżeli potrzebujesz bardziej obszernego procesu pielęgnowania pacjenta po udarze mózgu, możesz znaleźć go TUTAJ. Proces zawiera 30 stron, na których znajdują się:
✔️ przykładowy opis przypadku pacjenta po udarze niedokrwiennym mózgu – opis przypadku, indywidualny arkusz opisu przypadku, badanie fizykalne – 5 str.,
✔️ przykładowy proces pielęgnowania pacjenta, w tym 14 diagnoz wg V-etapowego modelu opieki pielęgniarskiej (diagnoza, cel opieki, plan, realizacja planu opieki i wynik podjętych działań) oraz 10 diagnoz wg modelu ICNP – 25 stron.


Jeżeli potrzebujesz więcej inspiracji z zakresu procesu pielęgnowania pacjenta, zerknij na proces opieki pielęgniarskiej nad pacjentem z cukrzycą oraz inne procesy pielęgnowania.
Źródła:
[1] Coupland AP, Thapar A, Qureshi MI, Jenkins H, Davies AH. The definition of stroke. J R Soc Med. 2017 Jan;110(1):9-12.
[2] Clarke E. Apoplexy in the hippocratic writings. Bull Hist Med 1963; 37: 301–314.
[3] Pound P, Bury M, Ebrahim S. From apoplexy to stroke. Age Ageing 1997; 26: 331–337. Schutta HS, Howe HM.
[4] Seventeenth century concepts of “apoplexy” as reflected in Bonet’s “Sepulchretum”. J Hist Neurosci 2006; 15: 250–268.
[5] Pearce JM. Johann Jakob Wepfer (1620-95) and cerebral haemorrhage. J Neurol Neurosurg Psychiatry 1997; 62: 387–387.
[6] Schutta HS. Morgagni on apoplexy in De Sedibus: a historical perspective. J Hist Neurosci 2009; 18: 1–24.
[7] Aho K, Harmsen P, Hatano S, Marquardsen J, Smirnov VE, Strasser T. Cerebrovascular disease in the community: results of a WHO collaborative study. Bull World Health Organ 1980; 58: 113–130.
[8] Sacco et al. An Updated Definition of Stroke for the 21st Century: A Statement for Healthcare Professionals From the American Heart Association/American Stroke Association. Stroke 2013;44(7):2064-2089.
[9] Chung JW, Park SH, Kim N, Kim WJ, Park JH, Ko Y, Yang MH, Jang MS, Han MK, Jung C, Kim JH, Oh CW, Bae HJ. Trial of ORG 10172 in Acute Stroke Treatment (TOAST) classification and vascular territory of ischemic stroke lesions diagnosed by diffusion-weighted imaging. J Am Heart Assoc. 2014 Aug 11;3(4):e001119.
[10] Parmar P. Stroke: Classification and diagnosis 2018;10(1):1-15.
[11] Feigin VL, Brainin M, Norrving B, Martins SO, Pandian J, Lindsay P, F Grupper M, Rautalin I. World Stroke Organization: Global Stroke Fact Sheet 2025. Int J Stroke. 2025 Feb;20(2):132-144.
[12] Kruk M., Pawlewicz A., NFZ o zdrowiu. Udar niedokrwienny mózgu w latach 2017-2022, https://ezdrowie.gov.pl/portal/home/badania-i-dane/zdrowe-dane/raporty/nfz-o-zdrowiu-udar-niedokrwienny-mozgu.
[13] Akindahunsi T., Ogunseye OO., Idowu O., Lawal T. Early signs of stroke: How your body warns you. World Journal of Advanced Research and Reviews 2019;3(2):091-100.
[14] Darkhabani MZ., Homa-Bonell JK., Thoreson L., Bobholz JA., Spauding D., Engebose M. BE FAST Versus FAST: A Randomized Pilot Trial Comparing Retention of Stroke Symptoms Between 2 Mnemonics. JAHA 2024;13(19).
[15] Woszczyk D., Kłosiewicz T. The clinical relevance assessment of ROSIER scale in emergency care. Medical Research Journal 2022;(7)3:249-255.
[16] Kummer von R. Time Is Brain: Fact or Fiction. Stroke 2019;50(3).552-553.
[17] Iverson M. Glasgow Coma Scale, StatPerals, 2023.
[18] Hinkle J. The NIHSS for International Neuroscience Nurses. The Journal of Neurological and Neurosurgical Nursing 2014;3(3):97–144.
[19] Podlasek A., Kobayashi A., Grunwald I.: Skala ASPECTS w udarze niedokrwiennym, Polski Przegląd Neurologiczny 2018;14(4):222–229.
[20] Schreiner T., Romanescue C., Schreiner O., i wsp.: Post-stroke aphasia management – from classical approaches to modern therapies, Ro J Neurol., 2022, 21(2), 103-109.
[21] Yang X., Shi L., Ran D., i wsp.: The treatment of post-stroke dysarthria with a combination of different acupuncture types and language rehabilitation training: a systematic review and network meta-analysis, Ann Transl Med., 2022, 10(23), 1281.
[22] Polit M., Chmielewska-Walczak J., Stopińska K., Domitrz I. Dysfagia ustno-gardłowa w ostrej fazie udaru mózgu – czynniki prognostyczne zaburzeń połykania oraz korelacja lokalizacji uszkodzenia OUN z objawami dysfagii. Logopedia 2021;50(1):49-65.
[23] Chohan SA, Venkatesh PK, How CH. Long-term complications of stroke and secondary prevention: an overview for primary care physicians. Singapore Med J. 2019 Dec;60(12):616-620.
[24] Dutta D., Sen S., Aruchamy S., Mandal S. Prevalence of post-stroke upper extremity paresis in developing countries and significance of m-Health for rehabilitation after stroke – A review. Smart Health 2022;23:100264.
[25] Konecny P., Elfmark M., Urbanek K. Facial paresis after stroke and its impact on patients’ facial movement and mental status. Journal of rehabilitation medicine: official journal of the UEMS European Board of Physical and Rehabilitation Medicine 2011;43(1):73-75.
[26] Sand KM., Midelfart A., Thomassen L., Melms A. Visual impairment in stroke patients – a review. Acta neurologica Scandinavica. Supplementum 2013;127(196):52-56.
[27] Kolmos M., Christoffersen LC., Kruuse C. Recurrent Ischemic Stroke – A Systematic Review and Meta-Analysis. Journal of Stroke and Cerebrovascular Diseases 2021;30(8):105935. [
[28] Lyden P.: Using the National Institutes of Health Stroke Scale A Cautionary Tale, Stroke. 2017;48:513-519.
[29] Li X, He Y, Wang D, Rezaei MJ. Stroke rehabilitation: from diagnosis to therapy. Front Neurol. 2024 Aug 13;15:1402729.
[30] Maier M., BAllester B., Verschule P.: Principles of Neurorehabilitation After Stroke Based on Motor Learning and Brain Plasticity Mechanisms, Front. Syst. Neurosci., 2019;13.
[31] Hoffman J., Zbonik M., Hoffman A., i wsp.: rola rehabilitacji w procesie leczenia pacjentów po przebytym udarze mózgu, Choroby XXI wieku – wyzwania w pracy fizjoterapeuty, Wydawnictwo Wyższej Szkoły Zarządznia, Gdańsk, 2017.
[32] Prasetyowati CD., Firmanda GI. Empowering Post-Stroke Patients to Improve Self-Care and Prevent Recurrent Stroke Using Stroke Empowerment Education. Jurnal Keperawatan Komprehensif 2024;10(2):579-586.
[33] Słodownik D., Skrzypek-Czerkow M., Roszman A., Kozłowska M. Proces pielęgnowania pacjenta po udarze niedokrwiennym mózgu – studium indywidualnego przypadku. Pielęgniarstwo Neurologiczne i Neurochirurgiczne 2012;1(2):76-82.
[34] Wójcik R., Adam A., Natora J., Sulisz I. Słodownik D., Skrzypek-Czerkow M., Roszman A., Kozłowska M. Proces pielęgnowania pacjenta po udarze niedokrwiennym mózgu – studium indywidualnego przypadku. Pielęgniarstwo Neurologiczne i Neurochirurgiczne 2012;1(2):76-82.. Geriatria 2021;15:95-101.

